
引言:
近年来,形态各异、功能丰富的纳米材料不断涌现,推动着抗肿瘤纳米生物材料的不断更新和发展。由于纳米尺寸效应,纳米生物材料在生物体内具更长的循环时间,并可通过高通透性和滞留效应(EPR效应)靶向到肿瘤位置。目前,通过分子自组装技术,人们可以制备**多种功能的纳米材料,实现癌症的精准诊断与治疗。但是,如何构建简便高效的纳米材料仍然是目前研究中的难点。
成果简介:
近日,尹梅贞教授团队报道了一种基于吲哚方酸菁染料的自组装纳米药物,并将之应用于深层光动力-化疗联合肿瘤治疗,同时提出了花菁分子“聚集增强光动力”的理论。通过分子设计引入多功能基团,并进一步研究分子的自组装以及解组装过程,为制备高效抗肿瘤纳米材料提供了一种新途径。相关成果以“A Size-Reducible Nanodrug with Aggregation-Enhanced Photodynamic Effect for Deep Chemo-Photodynamic Therapy”为题发表于国际顶尖期刊Angew. Chem. Int. Ed.(影响因子12.102)上。师资博后冀辰东为论文的第一作者,尹梅贞教授以及中国科学院高能物理研究所尹文艳副研究员为共同通讯作者。
该研究工作报道了一种多功能荧光纳米药物,将吲哚方酸菁分子分别与环状RGD多肽及抗癌药物喜树碱相偶联,该双亲性分子在水中自组装形成均一稳定的、粒径为90 nm的纳米药物PTN(图1)。该纳米药物表现出以下特点:
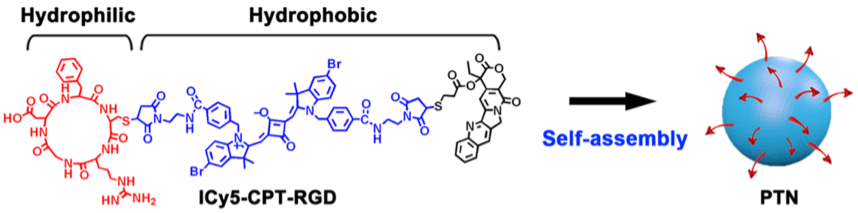
图1. 多功能靶向药物分子的化学结构及自组装形成PTN示意图
(1)光动力性能大大增强。由于吲哚方酸菁染料的聚集,染料分子的系间窜跃率增加(图2A, I),促进了PTN的光动力效应。与单分子相比,PTN的单线态氧量子产率提高了10倍,保证了纳米药物在光动力治疗过程中的功效。
(2)光照后尺寸可减小。光动力过程产生了大量单线态氧,导致部分吲哚方酸菁分子发生降解,进而导致纳米粒子的解组装。因此,光照会诱发纳米药物的尺寸缩减(图2A, II)。如图所示,光照10 min后,PTN的粒径由90 nm缩减至10 nm(图2B)。这种尺寸变化特性在药物递送至肿瘤过程中具有重要意义:90 nm的药物可以通过EPR效应在肿瘤部位富集,给予光照后,产生的小尺寸药物(10 nm)将更深入渗透到肿瘤组织中。因此,该纳米药物有望进一步应用于肿瘤的深层治疗(图2A, III-IV)。
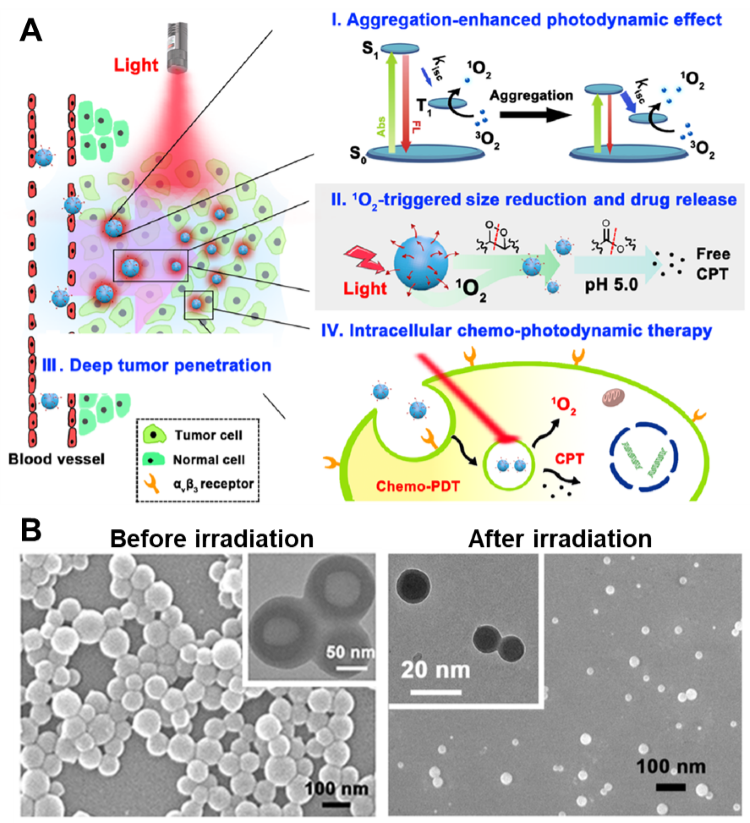
图2.(A)纳米药物“聚集增强光动力”效应(I)、尺寸缩减过程(II),肿瘤深度渗透(III)及癌细杀伤(IV)示意图。(B)光照前后PTN的扫描及透射(插图)电镜图片。
(3)实现多功能癌症诊疗。由于靶向基团RGD的引入,PTN在肿瘤部位富集时间大大延长。利用吲哚方酸菁的近红外荧光特性,PTN实现了对肿瘤的活体成像(图3A)。最终,该纳米药物实现了光动力-化疗联合疗法并有效抑制肿瘤的生长(图3B)
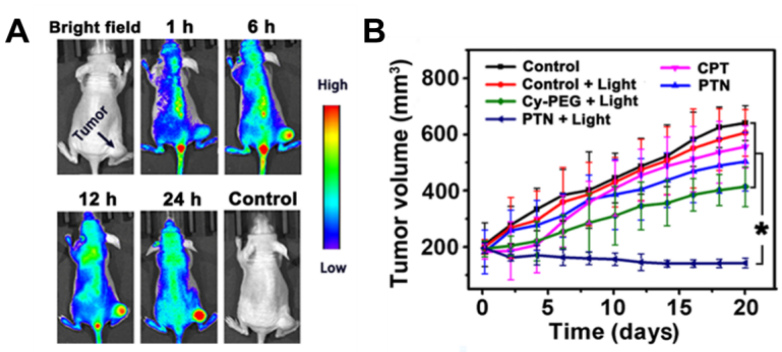
图3.(A)PTN用于对肿瘤的活体成像。(B)PTN用于光动力-化疗联合疗法****
该研究的最大意义在于:通过分子的自组装-解组装过程,该自组装纳米药物实现了 “聚集增强光动力”及光照尺寸缩减效应。该研究为制备多功能诊疗纳米材料提供了新思路。
论文链接:https://onlinelibrary.wiley.com/doi/abs/10.1002/anie.201807602
(Chendong Ji, Qin Gao, Xinghua Dong, Wenyan Yin*, Zhanjun Gu, Zhihua Gan, Yuliang Zhao, and Meizhen Yin*, A Size-Reducible Nanodrug with Aggregation-Enhanced Photodynamic Effect for Deep Chemo-Photodynamic Therapy, Angew. Chem. Int. Ed. 2018, 57(35), 11384-11388).